L’hyperarousal tiene svegli i tuoi pazienti con insonnia?
In passato, l’insonnia veniva considerata semplicemente come una “difficoltà a dormire” causata da condizioni sottostanti o da scelte di stile di vita.1 Tuttavia, i meccanismi del sonno e dell’insonnia non erano stati completamente compresi.
Mentre continuiamo ad esplorare la scienza del sonno, stanno emergendo nuove prospettive nella comprensione dell’insonnia. Evidenze recenti indicano che il disturbo da insonnia cronica è una condizione medica caratterizzata da una disregolazione neurobiologica sottostante, nota come hyperarousal.2,3

L’insonnia può essere scatenata da diversi fattori:2,4
(comorbidità, sesso, età, ecc.)


(genetica)



Le aree cerebrali che promuovono la veglia sono iperattive durante la notte.2,4,5
Figura adattata da Levenson JC, et al. 2015.
Scopri come l’insonnia cronica influisce sulla funzionalità diurna dei tuoi pazienti

Scopri il meccanismo alla base del disturbo da insonnia cronica
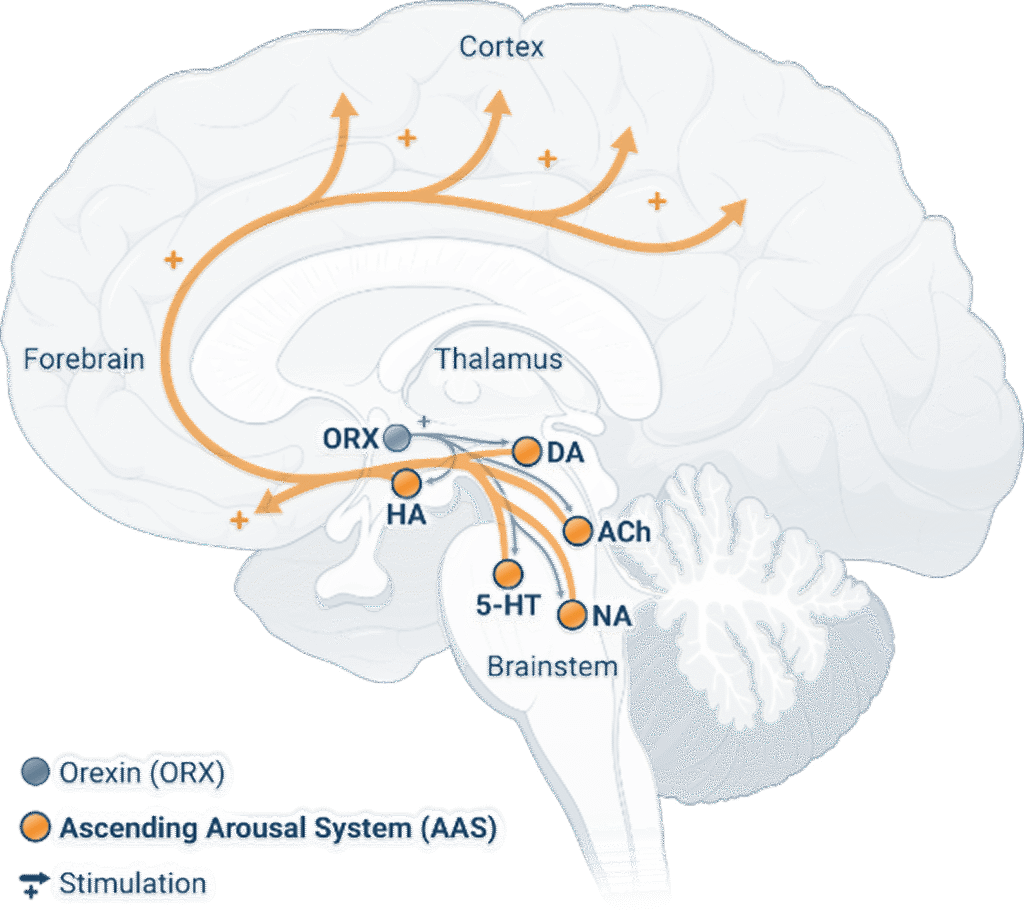
Sistemi che promuovono la veglia
Il sistema di attivazione ascendente è responsabile della regolazione dello stato di veglia.6
Durante il giorno, questo sistema rilascia neurotrasmettitori che promuovono la veglia nella corteccia cerebrale, generando attivazione neurologica e stato di veglia.6
L’orexina aiuta a mantenere lo stato di veglia rafforzando l’attività del sistema di attivazione ascendente durante il giorno, svolgendo così un ruolo cruciale nella regolazione della veglia.6,7
5-HT: serotonina; AAS: sistema di attivazione ascendente; ACh: acetilcolina; CNS: sistema nervoso centrale; DA: dopamina; GABA: acido γ-amminobutirrico; GAL: galanina; HA: istamina; NA: noradrenalina; ORX: orexina.
Disclaimer: queste immagini sono rappresentative di particolari stati nel cervello e delle principali aree coinvolte; non intendono essere una rappresentazione esaustiva di tutte le aree cerebrali implicate.
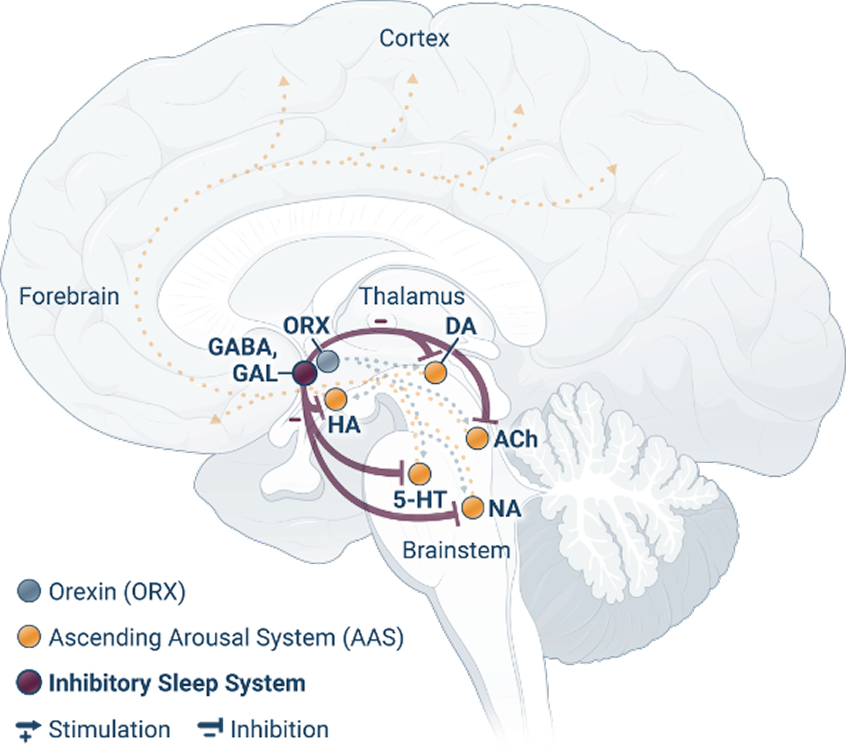
Sistemi che promuovono il sonno
Durante la notte, i neurotrasmettitori del sistema inibitorio del sonno inibiscono aree chiave del sistema di attivazione ascendente, favorendo lo stato di sonno.8
L’attività dei neuroni che rilasciano orexina diminuisce nella transizione al sonno, riducendo la stimolazione del sistema di attivazione ascendente e promuovendo così un sonno efficace.6,8
5-HT: serotonina; AAS: sistema di attivazione ascendente; ACh: acetilcolina; DA: dopamina; GABA: acido γ-amminobutirrico; GAL: galanina; HA: istamina; NA: noradrenalina; ORX: orexina.
Disclaimer: queste immagini sono rappresentative di particolari stati nel cervello e delle principali aree coinvolte; non intendono essere una rappresentazione esaustiva di tutte le aree cerebrali implicate.
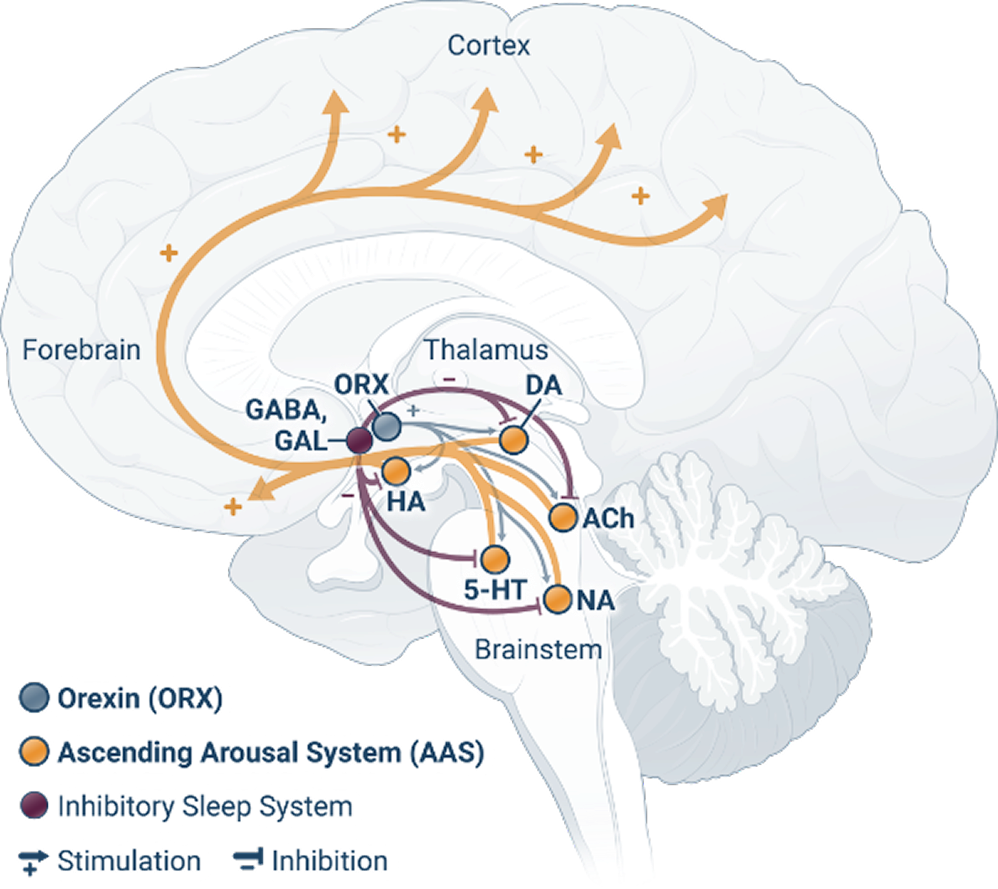
Stato di insonnia cronica
Nei soggetti con disturbo da insonnia cronica, le aree cerebrali responsabili della veglia rimangono attive. Questa eccessiva attivazione dei segnali di veglia durante la notte, nota come hyperarousal, compromette il sonno. 2,5,9
Poiché l’orexina promuove lo stato di veglia, potrebbe rappresentare un target specifico per il trattamento di persone con disturbo da insonnia cronica.10
5-HT: serotonina; AAS: sistema di attivazione ascendente; ACh: acetilcolina; DA: dopamina; GABA: acido γ-amminobutirrico; GAL: galanina; HA: istamina; NA: noradrenalina; ORX: orexina.
Disclaimer: queste immagini sono rappresentative di particolari stati nel cervello e delle principali aree coinvolte; non intendono essere una rappresentazione esaustiva di tutte le aree cerebrali implicate.
I trattamenti più comunemente prescritti per l’insonnia non agiscono direttamente sull’ hyperarousal6,11,12
• Sia le benzodiazepine che i farmaci Z inducono il sonno potenziando l’azione del principale neurotrasmettitore del cervello, il GABA6,12,13
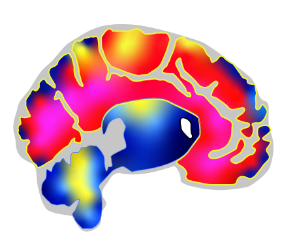

(pmol/ml)
Figura adattata da Nørgaard M, et al. 2021.
Scopri come l’insonnia cronica influisce sulla funzionalità diurna dei tuoi pazienti
Abbreviazioni e referenze:
5-HT: serotonina; AAS: sistema di attivazione ascendente; ACh: acetilcolina; CNS: sistema nervoso centrale; DA: dopamina; GABA: acido γ-amminobutirrico; GAL: galanina; HA: istamina; NA: noradrenalina; ORX: orexina.
1. Sharpley AL, et al. Int J Psychiatry Clin Pract. 1997; 1(2): 107–117.
2. Riemann D, et al. Sleep Med Rev. 2010; 14(1): 19–31.
3. Riemann D, et al. J Res Sleep. 2017; 26: 675–700.
4. Levenson JC, et al. Chest. 2015; 147(4): 1179–1192.
5. Nofzinger E, et al. Am J Psychiatry. 2004; 161: 2126–2129.
6. Saper C, et al. Nature. 2005; 437(7063): 1257–1263.
7. Janto K, et al. J Clin Sleep Med. 2018; 14(8): 1399–1408.
8. Saper C, et al. Trends in Neurosc. 2001; 24(12): 726–731.
9. Buysse D, et al. Drug Discov Today Dis Models. 2011; 8(4): 129–137.
10. Riemann D, et al. Lancet Neurol. 2015; 14: 547–558.
11. Matheson E, et al. Am Fam Psychiatry. 2017; 96(1): 29–35.
12. Dujardin S, et al. Sleep Med Clin. 2020; 15(2): 133–145.
13. Brambilla P, et al. Mol Psychiatry. 2003; 8(8): 721–737.
14. Shutte-Rodin S, et al. J Clin Sleep Med. 2008; 4(5): 487–504.
15. Nørgaard M, et al. Neuroimage. 2021; 232: 117878.
Materiale informativo destinato agli operatori sanitari.